diffusie - osmose - semipermeabel membraan - concentratie - osmotische waarde - isotoon - hypertoon - hypotoon - turgor - plasmolyse
Osmose: de verplaatsing van water
Elk molecuul in een vloeistof of een gas beweegt. Dit noemen we diffusie. Maar in de cel kunnen de meeste moleculen niet vrij bewegen. Ze worden geblokkeerd door membranen. Door het bestuderen van de cel weet je dat (bijna) elk organel en de cel zelf omsloten is door een membraan. Bijna alle stoffen moeten geholpen worden om door het membraan te kunnen, behalve zuurstof, koolstofdioxide en water. Water wordt overigens ook geholpen door speciale eiwitten genaamd aquaporines.
Osmose kun je diffusie van water noemen. Bij osmose is er sprake van membranen.
Een membraan van een cel laat dus sommige stoffen door en andere stoffen niet. Dit noemen we daarom een semipermeabel membraan (semi: half). Als je wilt weten hoe een membraan er uitziet, kijk dan hier.
Wanneer je over een oplossing spreekt, zoals een zoutoplossing, kun je het hebben over de concentratie zout in dze oplossing. De concentratie kun je uitdrukken in gram per liter of als een (massa)percentage. In een cel kun je moeilijk spreken over de concentratie opgeloste stoffen. Er zijn zeer veel opgeloste stoffen in een cel. Denk aan glucose, zuurstof, koolstofdioxide, aminozuren, eiwitten, afvalstoffen, ATP en nog veel meer. Alle opgeloste stoffen bij elkaar noemen we de osmotische waarde van een oplossing. Een oplossing met lage osmotische waarde bevat dus weinig opgeloste stoffen (en relatief veel water) en een oplossing met een hoge osmotische waarde bevat veel opgeloste stoffen (en relatief weinig water).
De definitie van osmose is: de verplaatsing van water van een hoge concentratie water naar een lage concentratie water over een semipermeabel membraan. Deze definitie is afgestemd op de definitie van diffusie.
Ook mogelijk zijn:
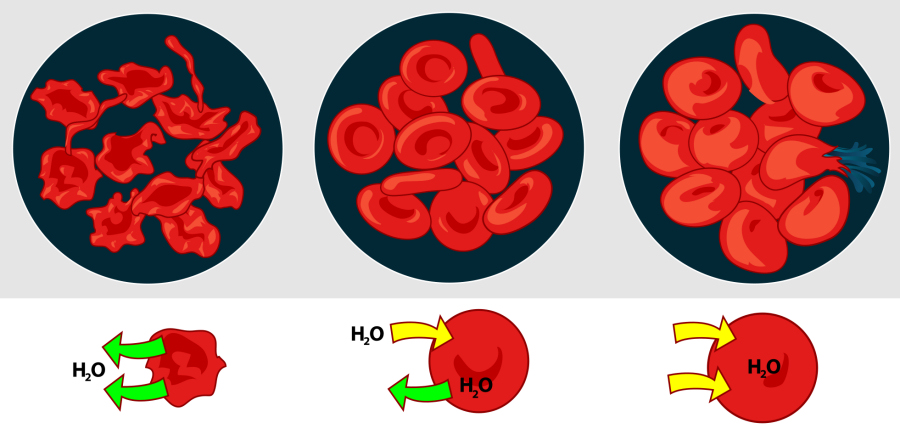
Een oplossing met een gelijke osmotische waarde noemen we isotoon. Een oplossing met een hogere osmotische waarde hypertoon en met een lagere osmotische waarde hypotoon.
Afhankelijk van de omgeving zal een cel dus water opnemen uit of afstaan aan de omgeving (zie figuur 1 en 2).
Osmose kun je diffusie van water noemen. Bij osmose is er sprake van membranen.
Een membraan van een cel laat dus sommige stoffen door en andere stoffen niet. Dit noemen we daarom een semipermeabel membraan (semi: half). Als je wilt weten hoe een membraan er uitziet, kijk dan hier.
Wanneer je over een oplossing spreekt, zoals een zoutoplossing, kun je het hebben over de concentratie zout in dze oplossing. De concentratie kun je uitdrukken in gram per liter of als een (massa)percentage. In een cel kun je moeilijk spreken over de concentratie opgeloste stoffen. Er zijn zeer veel opgeloste stoffen in een cel. Denk aan glucose, zuurstof, koolstofdioxide, aminozuren, eiwitten, afvalstoffen, ATP en nog veel meer. Alle opgeloste stoffen bij elkaar noemen we de osmotische waarde van een oplossing. Een oplossing met lage osmotische waarde bevat dus weinig opgeloste stoffen (en relatief veel water) en een oplossing met een hoge osmotische waarde bevat veel opgeloste stoffen (en relatief weinig water).
De definitie van osmose is: de verplaatsing van water van een hoge concentratie water naar een lage concentratie water over een semipermeabel membraan. Deze definitie is afgestemd op de definitie van diffusie.
Ook mogelijk zijn:
- De verplaatsing van water van een lage concentratie opgeloste stoffen naar een hoge concentratie opgeloste stoffen over een semipermeabel membraan.
- De verplaatsing van water van een lage osmotische waarde naar een hoge osmotische waarde over een semipermeabel membraan.
Een oplossing met een gelijke osmotische waarde noemen we isotoon. Een oplossing met een hogere osmotische waarde hypertoon en met een lagere osmotische waarde hypotoon.
Afhankelijk van de omgeving zal een cel dus water opnemen uit of afstaan aan de omgeving (zie figuur 1 en 2).
Een plantencel bezit een celwand en een vacuole, twee organellen die een dierlijke cel niet bezit. Video 2 laat duidelijk zien dat een celwand zo lek is als een mandje: er zitten gaten in. Een celwand houdt geen stoffen buiten, zoals een celmembraan, maar zorgt voor stevigheid. Een celmembraan is erg fragiel, maar houdt wel stoffen binnen en buiten de cel.
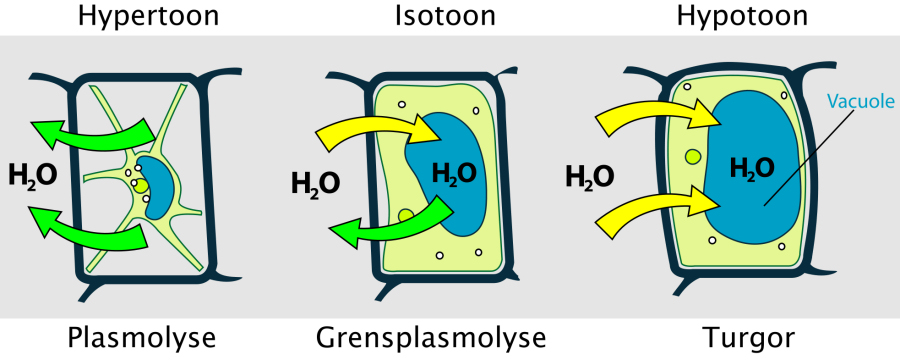
Door de celwand ontstaan er bij een plantencel turgor wanneer de plantencel water opneemt uit de omgeving. De osmotisch druk (water wordt opgenomen) zorgt voor het vullen van de vacuole en de verdere cel en de celinhoud drukt tegen de celwand aan. De celwand is hier tegen bestand. Een dierlijke cel zal steeds groter worden en uiteindelijk barsten (zie video 2).
In een hypertone omgeving zal een cel veel water verliezen. Een dierlijke cel wordt steeds kleiner en de celmembraan van een plantencel zal loslaten van de celwand. Dit proces noemen we plasmolyse en is onder andere mooi te bekijken bij de cellen van een rode ui.
Door de celwand ontstaan er bij een plantencel turgor wanneer de plantencel water opneemt uit de omgeving. De osmotisch druk (water wordt opgenomen) zorgt voor het vullen van de vacuole en de verdere cel en de celinhoud drukt tegen de celwand aan. De celwand is hier tegen bestand. Een dierlijke cel zal steeds groter worden en uiteindelijk barsten (zie video 2).
In een hypertone omgeving zal een cel veel water verliezen. Een dierlijke cel wordt steeds kleiner en de celmembraan van een plantencel zal loslaten van de celwand. Dit proces noemen we plasmolyse en is onder andere mooi te bekijken bij de cellen van een rode ui.
|
Video 1. het verschil tussen een gekookte en een ongekookte aardappel.
|
Video 2. het verschil tussen een plantaardige en dierlijke cel bij osmose
|
Terug naar Onderwerpen